Ο FDA εγκρίνει θεραπεία 3,2 εκατ. δολαρίων για σπάνια μυϊκή δυστροφία
28 Ιουνίου 2023, 07:00
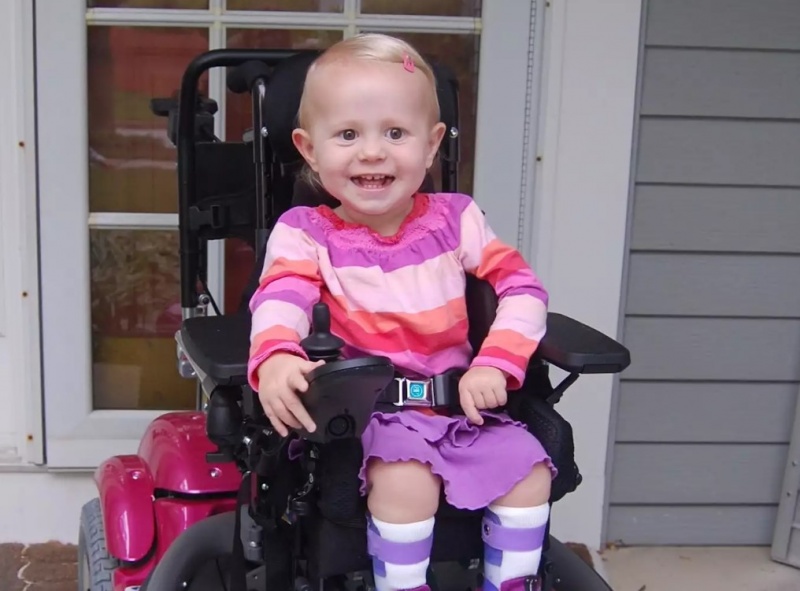
Ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) ενέκρινε την πρώτη γονιδιακή θεραπεία για τη θεραπεία μίας σπάνιας μυϊκής νόσου, αλλά περιόρισε την έγκριση σε παιδιά ηλικίας 4 και 5 ετών, με βάση τα διαθέσιμα στοιχεία.
Το φάρμακο, από την εταιρεία βιοτεχνολογίας Sarepta Therapeutics, καλείται να αποδείξει σε μία συνεχιζόμενη κλινική δοκιμή ότι βελτιώνει τη σωματική λειτουργία και την κινητικότητα σε ασθενείς με μυϊκή δυστροφία Duchenne, προκειμένου να παραμείνει στην αγορά, δήλωσε ο FDA.
Η Duchenne προκαλεί προοδευτική μυϊκή αδυναμία που μπορεί να στερήσει από τα παιδιά την ικανότητά τους να περπατούν μέχρι να φτάσουν στην εφηβεία και πολλά από αυτά δεν ζουν υπό φυσιολογικές και ευμενείς συνθήκες μέχρι τα 30 τους. Επηρεάζει περίπου 1 στα 3.300 αγόρια. Η Sarepta αναφέρει ότι η θεραπεία, που ονομάζεται Elevidys, θα κοστίσει 3,2 εκατομμύρια δολάρια ανά ασθενή. Είναι σχεδιασμένη να λαμβάνεται μόνο μία φορά.
Η ομάδα για την οποία εγκρίθηκε το φάρμακο, τα παιδιά ηλικίας 4 και 5 ετών, αποτελεί περίπου το 6% του πληθυσμού των ατόμων με Duchenne, σύμφωνα με τον Brian Abrahams, αναλυτή της εταιρείας RBC Capital Markets της Wall Street, που είχε υπολογίσει ότι η Sarepta θα κοστολογούσε το φάρμακο στα 2,8 εκατομμύρια δολάρια ανά ασθενή, κάτι που θα μπορούσε να αποφέρει έσοδα 2,1 δισεκατομμυρίων δολαρίων από την αρχική ομάδα που ήταν επιλέξιμη για το φάρμακο.
«Η σημερινή έγκριση αντιμετωπίζει μια επείγουσα ανικανοποίητη ιατρική ανάγκη και αποτελεί σημαντική πρόοδο στη θεραπεία της μυϊκής δυστροφίας Duchenne, μιας καταστροφικής κατάστασης με περιορισμένες θεραπευτικές επιλογές, που οδηγεί σε προοδευτική επιδείνωση της υγείας ενός ατόμου με την πάροδο του χρόνου», δήλωσε ο Δρ. Peter Marks, διευθυντής του Κέντρου Αξιολόγησης και Έρευνας Βιολογικών Φαρμάκων του FDA, ανέφερε στο δελτίο τύπου του οργανισμού. «Ο FDA παραμένει προσηλωμένος στη διευκόλυνση της ανάπτυξης καινοτόμων νέων θεραπειών για τη μείωση του αντίκτυπου των εξουθενωτικών ασθενειών και για τη βελτίωση των αποτελεσμάτων και της ποιότητας ζωής για όσους επηρεάζονται».
Τέλος, η Sarepta ενημέρωσε ότι τα πρώτα αποτελέσματα από την επιβεβαιωτική δοκιμή του φαρμάκου, αναμένονται στα τέλη του έτους.